Elektrotechnik für Elektroberufe
Kartei Details
| Karten | 33 |
|---|---|
| Sprache | Deutsch |
| Kategorie | Elektrotechnik |
| Autor | Paul Baumgartner |
| Stufe | Berufslehre |
| Copyright | |
| Zielgruppe | |
| Erstellt / Aktualisiert | 21.04.2017 / 23.06.2025 |
| Druckbar | Ja |
Sammlung
Diese Kartei ist Teil der Sammlung Elektrotechnik für Elektroberufe
Welche Bemessungsspannung liefern herkömmliche Lithium-Ionen-Akkumulatoren?
3,6 V (dies ist dreimal so viel, wie ein NiMH-Akkumulator!)
Wofür werden Lithium – Ionen – Akkumulatoren eingesetzt?
Für kleinere elektronische Geräte, wie Handys, Notebooks, Digitalkameras usw.
Welcher Akkumulatorentyp wird in Zukunft am meisten verwendet werden?
der Lithium-Ionen-Akkumulator
Er könnte sich auch als Stromspeicher in Kombination mit Photovoltaikanlagen durchsetzen.
Nennen Sie einige Beispiele, wo KEINE NiMHAkkumulatoren verwendet werden sollten.
Uhren, Feuermelder, Taschenlampen, Fernbedienungen.
Warum sind NiMH-Akkumulatoren umweltverträglicher als NiCd-Akkumulatoren?
Sie enthalten kein giftiges Cadmium. (Aus diesem Grund gibt es auch keinen Memory-Effekt)
Bei welchem Akkutypen kann der Memory-Effekt auftreten?
NiCd-Akkumulator
Die Bedeutung des Memory-Effektes hat in den letzten Jahren stark abgenommen, weil anstelle der Ni-Cd-Akkus immer mehr Ni-MH-Akkus (Nickel-Metallhydrid-Akkus) eingesetzt werden.
Weshalb müssen NiCd-Akkumulatoren speziell entsorgt werden?
Cadmium ist ein giftiges Schwermetall.
Wo werden NiCd-Akkumulatoren eingesetzt?
Allgemein für Hochstromanwendungen (kleiner Innenwiderstand), wie Akkuschrauber, Modellbau usw.
Wie verhält sich die Dichte des Elektrolyten eines NiCd-Akkumulators während dem Lade- bzw. Entladevorganges?
Die Dichte ändert sich nicht. Anhand der Dichte kann keine Aussage bezüglich des Ladezustandes gemacht werden.
Was wird bei einem NiCd-Akkumulator als Elektrolyt verwendet?
Verdünnte Kalilauge (KOH + H2O)
Warum gefriert eine entladene Akkumulatorenbatterie schon bei -10... -5°C?
Weil die Säuredichte klein ist (viel Wasser!). Je mehr Wasser, desto näher liegt der Gefrierpunkt des Elektrolyten bei 0°C.
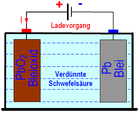
Woraus (Teile, Material) besteht ein Bleiakkumulator?
mindestens 2 Bleiplatten Elektrolyt (verdünnte Schwefelsäure) Gefäss, Klemmen, Verbindungsmaterial, Separatoren
Was geschieht spezielles im Elektrolyten beim Ladevorgang eines Bleiakkumulators?
Die Säuredichte steigt.
Was wird als Elektrolyt verwendet bei einem Bleiakkumulator?
Schwefelsäure + Wasser (H2SO4 + H2O)
(verdünnte Schwefelsäure)
2 V
Amperestunden [Ah]
Grosse Lebensdauer (10 Jahre), hoher Preis, geringe Selbstentladung, Leerlaufspannung 1,5 V – 3,5 V
Welche Eigenschaften haben alkalische Zink-Mangandioxid-Zellen?
Geringe Selbstentladung, hohe Belastbarkeit, hohe Energiedichte.
Leclanché Zellen sind auch unter der Bezeichnung Kohle-Zink-Batterien bekannt. Wie gross ist gemäss elektrochemischer Spannungsreihe die Leerlaufspannung U0 einer Zink-Kohle-Batterie?
1,5 V (Kohle + 0,74 V und Zink – 0,76 V)
Mit welchen Massnahmen lässt sich elektrochemische Korrosion vermeiden?
- Verwendung von Schutzstrom z. B. „Opferelektrode“ (unedlere Elektrode in Wassererwärmern)
- Unterbrechung des Korrosionsstromes z. B. Isolierung beider Metalle oder Verwendung gleicher Metalle
- Wahl geeigneter Metalle mit kleiner Spannungsdifferenz z. B. Verzinken von Stahlschrauben
Die Korrosionsgefahr ist umso grösser, je weiter die Metalle in der elektrochemischen Spannungsreihe auseinander liegen, je stärker der Elektrolyt ist und je besser sich Luft im Elektrolyten lösen kann.
Ein Metall ist umso unedler, je höher sein Lösungsdruck ist. D.h. je schneller sich das Metall auflöst. Allgemein ist ein Metall unedel, wenn das Potenzial gegenüber der NormalWasserstoff-Elektrode negativ ist.
Was versteht man unter eloxieren?
Elektrolytische Oxidation von Aluminium, d.h. verstärken der Oxidschicht.
Was versteht man unter galvanisieren?
Überziehen eines Metalles mit einem anderen, auf elektrolytischem Wege.
Beispiele: verkupfern, vernickeln, verzinken (ERZ-Rohr: Verzinktes Eisenrohr)
Ionen sind elektrisch geladene Atome oder Atomgruppen. Sie entstehen durch Abgabe oder Aufnahme eines oder mehrerer Elektronen.
Warum leitet reines Wasser, wenn Kochsalz beigemischt wird?
Durch das Kochsalz gelangen Ladungsträger in das Wasser.
Warum leitet destilliertes Wasser nicht?
Weil es keine Ladungsträger (Ionen) enthält.
Wie nennt man elektrisch leitende Flüssigkeiten?
Man nennt sie Elektrolyte.
Dazu gehören wässrige Lösungen von Säuren, Basen, Salzen und deren Schmelzen.